前回、サンバイオの慢性期脳卒中治療薬「SB623」についての記事で少しだけ治験についても触れました。
今回はSB623の進捗と絡めながら「治験」とは何かを整理をしてみましょう。
治験とは新薬承認のために行われる臨床試験です。
私達患者側から見ると、治験には既存の薬や治療法では治癒が困難な疾患を未承認薬を使って治す手段という側面も持ち合わせています。しかし、治験に参加しても必ずしも未承認薬を投与されるわけではありません。
これはどういうことなのでしょうか?
新薬承認までの手順
薬はいくつもの段階を経て新薬として承認されます。
まずは承認までの流れを知っておきましょう。
0)動物実験
新薬開発はまずマウスなどの動物を用いて試されます。
動物で効果や副作用を確認できたところで人に対しての臨床試験「治験」に移ります。
1)フェーズ1(第一相)
まだ有効性/安全性が証明されていない新薬候補を初めて人に投与する試験であり、対象は患者ではなく健康な方です。このフェーズでは薬の適切な投与量や手段を見出すために血液中濃度や排泄量の測定が行われます。
「薬飲んで部屋でゴロゴロ、たまに採血採尿するだけの超高額バイト!!」の正体はコレです。
2)フェーズ2a(第二相前半)
フェーズ2から患者に対しての治験です。
フェーズ1で得た用量と期間の目安をもとに、患者に対しての投与条件を見極めるための試験です。効果と副作用の関係を確認して投与条件の候補を絞り込みます。
ここまでは比較的小規模な治験です。
慢性期脳梗塞の治療薬としてのSB623は現時点でこの2aまで終了しています。
3)フェーズ2b(第二相後半)
投与条件のさらなる絞り込みとプラセボ(偽薬)との比較が行われます。
プラセボ効果とは、偽薬でも「薬を飲んだから治る」と強く信じることで効果が、そして副作用までもが出てしまう現象です。このため一般的に「二重盲検」という手法が用いられます。患者だけでなく医師も新薬か偽薬か分からない状態で治験が進められます。プラセボ効果による変化との差を見て、新薬が安全で効果があるかを判断するわけです。
つまり治験を受けても新薬の投薬が約束されるわけではないのです。
ただし、患者が従来の治療で回復するはずの機能を失うような治験は許可されません。例えば抗がん剤や降圧剤を完全に止めて異なるアプローチを持つ新薬を試すなどのリスクの高い治験は出来ないということです。この場合は新薬を従来の治療に加えるという手法が取られます。これによりたとえ偽薬であったとしてもそれは従来の治療と同じであり、治験に参加した患者にもデメリットにはなりにくいという配慮です。
フェーズ3(第三相)
従来の薬と新薬候補を比較する大規模な治験です。
ここでもどちらの薬を投与されるか分からない「実薬対照二重盲検」で実施されます。 ここで従来薬よりメリットがあると判断されるとめでたく新薬承認となります。
ただしフェーズ3は必要とあれば長期間服用の影響も確認します。このことが承認まで時間を要する原因の一つとされています。
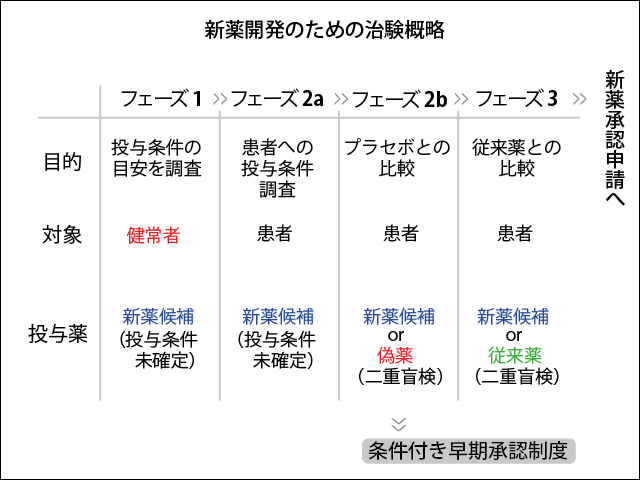
なお、上記は一般的な新薬開発に対してのものであり、治験の内容は疾患や薬などの事情で調整がなされます。例えば現時点では慢性期脳卒中治療薬は存在しません。従来薬との比較試験ができないので、SB623にフェーズ3があったのなら大規模な偽薬対照の二重盲検になったのかも知れません。
つまり新薬が投与されるとは限らない
未承認の新薬投与を望んで治験に参加しても必ず新薬を投与されるわけではないということです。治験期間終了後に「実はあなたに投与したのは偽薬でした」と無情な宣告をされる場合もあるのです。
条件付き早期承認制度
おそらく皆様もご存知のとおり、近年国内で新薬の条件付き早期承認制度が整備されました。
この制度のポイントは上記フェーズ2b終了の段階で条件付き承認としてしまう点です。
2bで効果と安全性の目安がつき、さらに社会的需要が高いと判断される新薬はこの制度によりフェース3を飛ばして短い期間で実用化されるということです。
「条件付き承認」ですので、付与された条件で限定された実用化ではありますが、盲検ではないため必ず新薬が投与されます。
サンバイオの脳卒中治療薬「SB623」もこの制度を活用しようとしています。これから実施される慢性期脳卒中に対する治験「フェーズ2b」が良い結果でまとまれば、この薬は世界に先駆けて日本で初の実用化ということになるでしょう。
ではいつまで待てばよいのでしょうか?
SB623が慢性期脳梗塞治療薬として承認されるのは最短でいつか?
サンバイオは平成32年(2020年)1月期中の承認申請を目標としています。
最新情報はサンバイオIRニュースの「再生細胞薬「SB623」の開発進捗総括の更新について」でご確認ください。
新薬申請から承認までの期間は年々短縮されており、近年では通常品目の70%が12ヶ月以内、優先品目の70%が9ヶ月以内という実績があります。SB623には早期承認制度を活用するというイレギュラーな部分もありますが全てが順調に進んだ場合、最短の承認は2020年10月と予想しています。
しかし早期承認制度を活用することで治験への募集が滞ることも想定できます。新薬承認が早いのであれば数年待って確実に新薬を投与されることを選ぶ方が増えるでしょう。SB623の承認時期見極めはフェース2bの開始時期ではなく、募集人数が集まり投薬組入れ完了がいつになるかが大きなポイントになりそうです。
そして「条件付き承認」ですのでどのような条件が付与されるかも重要です。承認後も安全性や有効性を追跡することは間違いないでしょうが、投薬/施術の施設を絞り込まれてしまうと患者が集中し治療がなかなか受けられない事態に陥ることも考えられます。付与される「条件」も重要なポイントですので気にしておきましょう。
治験の負担軽減費/費用について

未承認薬は基本的に保険対象外ではありますが、この新薬治験部分の費用は病院持ちとなります。つまり治療中の患者の場合、標準的な治療部分は保険適用で患者持ち、新薬部分は病院持ちとなります。治験期間中の医療費を全額負担してくれるわけではありません。
そして一般的に、治験によって生じる通院/入院には負担軽減費が支払われています。1通院に対して7000円、入院1泊に対して10000~20000円が目安と言われています。
ここで注意したいのは「治験によって生じる負担に対して」という名目です。具体的には本来発生しないはずの交通費や拘束時間、生活制限を意味します。つまりもともと入院が必要な方には負担軽減費が支払われない場合もあるのです。
このような仕組みのため、健康な方がフェース1に参加する場合は高額の収入にもなり得ます。しかし治療中の患者の場合、その名目通り負担を軽減する程度の扱いになってしまうかもしれません。
私達の目的は完治です。治験による臨時収入を期待するのはやめておきましょう。
ともあれ、負担軽減費の金額は患者の状態と治験の種類、病院により変化します。治験への参加を検討しているのであれば事前にしっかり確認をしておきましょう。
脳出血やクモ膜下出血への展開は?
現在SB623で行われている治験は外傷性脳障害と慢性期脳梗塞で、早期承認を目指しているのは慢性期脳梗塞の治療薬です。つまり承認が下りたとしても脳出血やクモ膜下出血の患者はこの新薬による治療が受けられないということになります。
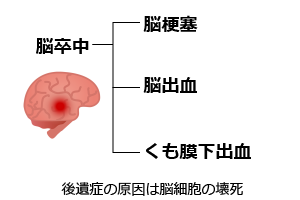
発症の仕組みは異なりますが、麻痺などの後遺症は脳細胞が部分的に壊死することで生じている点は同じです。まずは疾患を絞り込んで新薬の承認を得て、そこから対象疾患を広げていくものと考えられますが、この点についてサンバイオからの案内は何もありません。
後遺症の原因は共通していますので承認薬の適応外使用という可能性もゼロではありません。しかし条件付き承認がされたばかりの実績がない新薬に適応外使用が許されるのか、未承認薬として高額の費用がかかるのではないか、医師がそこまで踏み込んでくれるのか、などが一切不明です。
脳出血経験者の一人として、サンバイオにはこの点を明確にしてほしいと切に願います。
最後に
以上が治験についての説明とSB623の状況です。
では、SB623の治験フェーズ2bに参加すべきでしょうか?
これはやはり患者次第です。
新薬承認までの期間は格段に短くなりそうです。しかし承認直後に全ての希望者が新薬治療を受けられるわけではないでしょう。そして私達中高年に残された時間は多くありません。後遺症で毎日耐え難い苦痛を感じているならなおさらです。
治験に参加するか否かはご自分の条件で総合的に考え、ご自分で決断をしてください。
今のあなたにはその選択が正解です。












コメント
私は2007.3.10右脳被殻出血により人生が180度あわった53歳男性です。
これまでにとにかく色々な先生にお話しをお聞きしました。
もとになることは、ありえません。同残りの人生を過ごせばよいのだろうか?
仕事にも限界があります・左片麻痺なのですから、
若い時に取った大型・大特面寄与もなく収入もなく、早急に脳内出血にもSB623の適応を望みます
はじめまして。
管理人のameoと申します。
コメントありがとうございます。
SB623は仕組みからしても脳梗塞にだけ効果があるものではないでしょう。
脳出血でも期待していいと思います。
ただ、開発ロードマップに脳出血に関しての記述が全く無いというのはどうにも解せません。
初めに脳梗塞で新薬承認を取得するにせよ、脳出血に関してもなにかコメントが欲しいですよね。
ameoさん、ご無沙汰しています。元気にしてらっしゃいますか?何度かサイトをチェックしたのですが記事の更新がなく、お仕事が大変なのかと心配しております。
私は脳内出血の後。幸い身体に麻痺もなく、順調に回復しているように見えたのですが、4年経って、自分が変わってしまったことに気づきました。それがなんなのか分からず、言葉を聞いても記憶に残らない、電話番号が分からない、人の名前が入ってこない、人の生活そのものに関心がなくなったなど、病気の前はあんなにおしゃべりで快活だった私が、家にこもりがちになり本当に一変してしまいました。同じ病気を発症した皆さんも、きっと経験があるのではないですか?
それが高次脳機能障害と呼ばれるものであること、去年の暮れにネットで見つけて、これだったのか!とスッキリしました。多分、調べる言葉が悪くて、ヒットしなかったんでしょうが、病名がわかれば、どう治療していくかは容易に探せます。試しにやってもらったのが、鍼治療です。
話が長くなってすみません。これも去年10月に車6台の追突事故に巻き込まれまして、むち打ちの治療にカイロプラクティックとマッサージ、そして鍼に通い始めました。中でも鍼がとても良かったので、高次脳機能障害のことを話し、試しに頭に鍼を打ってもらったんです。今はまだ治療の途中なので、なんとも言えませんが、自分ではどうしようもない症状に悩んでいるなら、試す価値はあると思います。薬が出来るまで、待っていられない。少しでも効果があるなら、なんでも試したい、そんな方にお勧めかもしれません。人によって症状は違うので、信頼できる先生と相談してくださいね。
お久しぶりでございます。
永いこと更新が止まっており申し訳なく思います。
私も同じような悩みを抱えています。
文章を読んでも概念の解釈に時間がかかったり、文字がなかなか頭に入ってこなかったり。
暗算が苦手になっていたり、集中が続かなかったりと。
全く出来ないわけではないのですがとにかく時間がかかるのです。
あとは年齢による影響もあるとも考えています。
残念なことではありますが私はもうしばらくすると高齢者です。
使われない機能から閉じていく時期でもあります。
それらが仕事の足を引っ張るのです。
私も自分のことを「変わってしまったなぁ」と寂しく思っています。
ただ、脳障害であれ加齢であれ、苦手になったから使わないは悪手です。
意識に関わるリハビリも手足のリハビリと仕組みは同じで、繰り返し使うことで脳に新しい神経回路ができ回復するのです。
なにか新しいことを始めてみてはいかがでしょうか?
是非楽しみながらリハビリができる趣味を見つけましょう。
私はまだまだあがきます。
再発しなくても経済的に退場となってしまいますので。
毎日楽しい老後のために今は頑張らないと。
一緒に頑張りましょう!!
ameoさん、良かった〜。ここでしか連絡出来ないので、思いきってメールをしたんですが、安心しました。
私もameoさんと同じような問題を抱えていました。外からは何も変わらないので、高機能機能障害になった人は徐々に引きこもりがちになり、鬱病を発症するケースも多いと聞きます。私も病後すぐの混沌とした生活から、だんだん自分の置かれた状況がハッキリしてくるにつれ、もう1人でもいいやと思ったり、かなり鬱気味になっていました。左脳の一部が壊れたのですが、どういう症状が出るかは人それぞれです。でも、一旦壊れた脳はそのままでも、別のラインで繋がることが出来ると聞きました。良いと聞いたら、なんでもやりたくなるんです。
去年日本に帰った時、百人一首のなぞり書きの本を買ってきて、せっせとやってきましたが、ようやく本に載っている41首を覚えたところ。私はameoさんより、年上です。年齢と共に忘れっぽくなるのは仕方ないと思いますが、それだって対処方はあるのかもしれません。
私が出会った鍼の先生は、香港から来られた方でしたが、使っている鍼は日本の鍼のように細いものでした。事故の後、調子が良くなってきたので、高次脳機能障害についてもなんとかならないか?と相談しました。
脳の中で、切れてしまったシナプスを刺激によって繋いでもらう、そういう感じでしょうか。諦めないで、お互い頑張りましょう❣️
本当にそうですね。
諦めるなんてもったいないです。
こうして会話をして、そのことを覚えている。
これは脳に新しい神経回路が出来ていることの証明です。
鍼を試すことを決断したこともそうですよ。
私達の脳は「生きていくために必要」と強く願えばまだまだ変化します。
新しいものに興味を持ち挑戦してみる。
脳が衰えない高齢者にそんな方が多いのも納得できますよね。
私達もそうありたいものです。
ameoさんを見つけて1年ちょい。悩んでた私に、希望の光を見出させてくれた方です。お互いにより良い人生を送るために頑張りましょうね。